云准医药科技(上海)有限公司
入驻年限:5 年
- 联系人:
刘女士
- 所在地区:
上海 徐汇区
- 业务范围:
技术服务、耗材、实验室仪器 / 设备、抗体、试剂
- 经营模式:
生产厂商 代理商
推荐产品
公司新闻/正文
多重免疫荧光技术应用于肿瘤药物开发 | 胰腺导管腺癌铁死亡抵抗关键通路及其机制研究
人阅读 发布时间:2024-04-22 17:58
2023年7月,中国医科院协和医学院于双妮及陈杰团队研究团队在《Cell Death & Differentiation》(IF=12.4)杂志上发表研究文章“Targeting N-glycosylation of 4F2hc mediated by glycosyltransferase B3GNT3 sensitizes ferroptosis of pancreatic ductal adenocarcinoma”。文章揭示了糖基转移酶B3GNT3介导的4F2hc N-糖基化可使胰管腺癌铁凋亡易发。
该研究发现谷氨酸-胱氨酸反转运系统Xc-的一个亚基4F2h,它的天冬酰胺(N)糖基参与了PDAC铁凋亡。通过敲低SLC3A2 (4F2hc的基因名称)或阻断4F2hc的N -糖基化,损害Xc-系统的活性会增强PDAC细胞对铁死亡的敏感性,导致细胞内谷胱甘显著减少。糖基转移酶B3GNT3催化4F2hc的糖基化,稳定4F2hc蛋白,增强4F2hc与xCT的相互作用。敲除B3GNT3或去除B3GNT3酶活性使PDAC细胞对铁死亡敏感。重组具有4F2hc缺陷细胞和野生型4F2hc细胞可恢复对铁凋亡的抗性,而与糖基化突变的4F2hc细胞重组则不能。
此外,在与铁死亡诱导剂联合使用时,经典N-糖基化抑制剂衣霉素 (TM)显著触发脂质过氧化的过度激活,并增强PDAC细胞对铁死亡的敏感性。SLC3A2的遗传干扰或与TM联合治疗显著增强了铁中毒诱导的原位PDAC抑制。临床上,4F2hc和B3GNT3的高表达与PDAC患者的进展和生存期差有关。
总之,研究结果揭示了先前未被认识到的4F2hc N -糖基化在铁死亡中的功能,并表明双重靶向N -糖基化缺陷和铁死可能是PDAC的一种创新治疗策略。
研究背景
铁死亡是近年来发现的一种铁和活性氧(ROS)依赖的调节性细胞死亡形式,它是不同于细胞凋亡、细胞坏死、细胞自噬的新型细胞死亡方式。其细胞致死原理是通过脂质过氧化产物的无限制毒性积累和质膜破裂实现。研究表明,铁死亡可能参与癌细胞死亡、神经毒性、神经退行性疾病、急性肾功能衰竭、药物性肝毒性、肝脏和心脏缺血/再灌注损伤和T细胞免疫等生命过程。在参与铁死亡防御的众多调控途径中,谷氨酸-胱氨酸反转运系统Xc-是最有名的,它由两个亚基组成,即重链亚基4F2hc(也称为CD98hc,由SLC3A2基因编码)和轻链亚基xCT(由SLC7A11基因编码),它们介导半胱氨酸衍生抗氧化剂的合成。
胰腺导管腺癌(PDAC)占胰腺癌病例的90%以上,通常危及生命,5年相对生存率约为11%。由于其较高的发病率和死亡率,预计到2040年,PDAC将成为癌症相关死亡的第二大原因。越来越多的证据表明,靶向铁死亡是可利用的癌症特征,特别是在PDAC中,由于它与KRAS突变驱动的抗氧化系统激活密切相关,并且富含铁,预示着它很可能通过诱导铁死亡使患者获益。先前的临床前研究表明,抑制外源性途径中的Xc-系统(如Xc-系统抑制和半胱氨酸消耗),或直接降低内在途径中核心抗氧化分子的活性或表达(如靶向GPX4、FSP1和DHODH的抑制剂)可促使PDAC细胞诱发生铁死亡。由于铁死亡抵抗和其他一些未知的潜在机制,这种治疗策略的成功率仍然有限。因此,更深入地了解铁死亡抵抗机制,可能会揭示新的相关通路,并为PDAC治疗提供更优化的方案。
研究过程
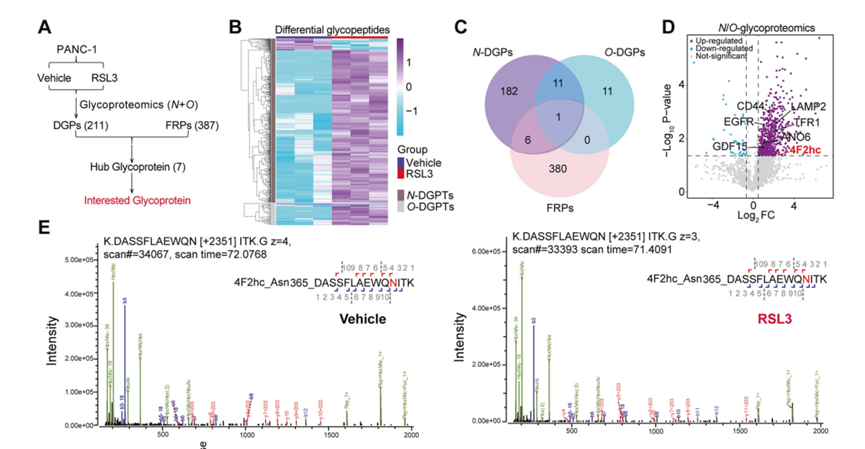
1.N-/O-糖蛋白组学和RNA-seq显示N-糖基化的4F2hc和糖基转移酶B3GNT3与PDAC死亡有关
RSL-3是一种过氧化物酶 4 (GPX4) 抑制剂, 铁死亡诱导剂。RNA测序表明,RSL-3处理后的PDAC细胞N-和O-糖基化相关基因的表达上调。GO和KEGG分析表明N-糖基化相关通路与癌症相关,其中4F2hc等七个基因显示可能具有关键作用。研究人员利用液相二级质谱(LC-MS-MS)对4F2hc基因进行研究,结果显示PDAC细胞中的4F2hc是一个高度N-糖基化的蛋白,并在铁死亡中发挥重要作用。进一步对转录组数据进行分析,发现B3GNT3可能是铁死亡反应的潜在调节剂,并可能涉及4F2hc的N -糖基化。
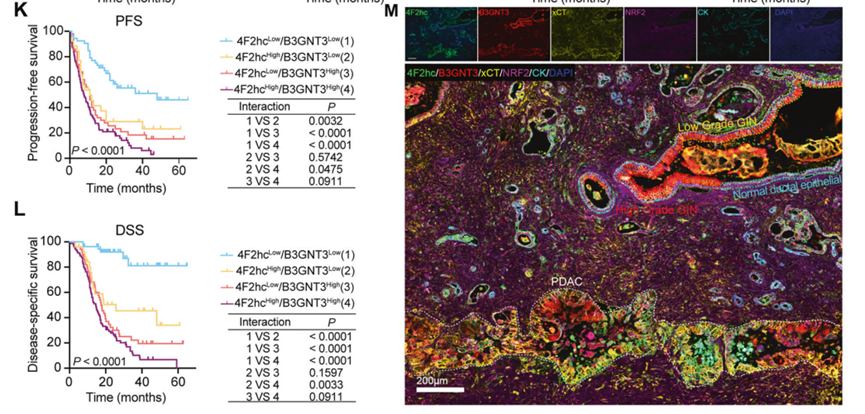
2. 4F2hc和B3GNT3都与PDAC的发展和预后有关
4F2hcs是氨基酸转运体中重要的伴侣蛋白。对PDAC患者肿瘤组织进行研究,发现与正常组织相比,肿瘤组织中的4F2hc和B3GNT3表达水平更高。4F2hc和B3GNT3的高表达与更差的无进展生存期(PFS)和疾病特异性生存期(DSS)相关。
多重免疫荧光实验发现,在细胞角蛋白(CK)阳性的上皮细胞中检测到4F2hc和B3GNT3,两者在空间上相互作用,并在相似的区域广泛定位。研究人员还观察到B3GNT3的表达随着腺上皮内瘤变的进展而逐渐增加,而在PDAC中略有下降。
3. 去除4F2hc的N -糖基化使PDAC细胞对铁死亡损伤敏感
4F2hc和xCT之间的相互作用通过增加细胞内胱氨酸内流和随后的谷胱甘肽(GSH)/GPX4系统的积累来阻碍铁死亡。CTRP数据库中的数据显示,SLC3A2与GPX4抑制剂如RSL3、ML162和ML210的耐药呈正相关,特别是在RLS3处理的胰腺癌细胞系中。阻断4F2hc的n -糖基化可使PDAC细胞对铁死亡敏感。
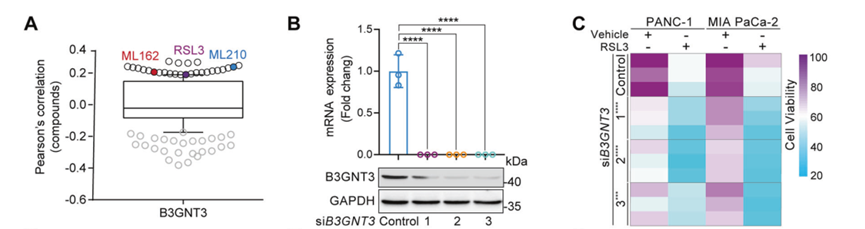
4. 受损的B3GNT3通过调节N -糖基化4F2hc的稳定性使PDAC细胞对铁死亡敏感
B3GNT3的高表达与对RSL3、ML162和ML210等铁死亡诱导剂的抗性呈正相关,特别是在RSL3处理的胰腺癌细胞系中。敲低B3GNT3可使PANC-1和MIA PaCa-2细胞对RSL3诱导的铁死亡更加敏感。GPX4在B3GNT3敲除细胞中的表达比Cas9d对照细胞中的表达转换更快,这表明B3GNT3对GPX4介导的糖基化调节存在潜在的质量控制机制。B3GNT3通过N-糖基化修饰促进非糖基化(NG) 4F2hc转化为糖基化(G) 4F2hc,稳定N-糖基化4F2hc,从而增强4F2hc介导的铁凋亡抗性。
5. N -糖基化稳定PDAC细胞中的4F2hc
此前有研究表明,在糖蛋白中去除N-聚糖会导致结构不稳定。研究人员使用在MD模拟,利用DynaMut和PredyFlexy预测了4F2hc的N -糖基化位点的蛋白稳定性和柔韧性的变化。结果表明,Asn365和Asn424突变导致4F2hc蛋白不稳定。进一步研究显示,去糖基化的4F2hc蛋白是不稳定的,可能更容易被降解。
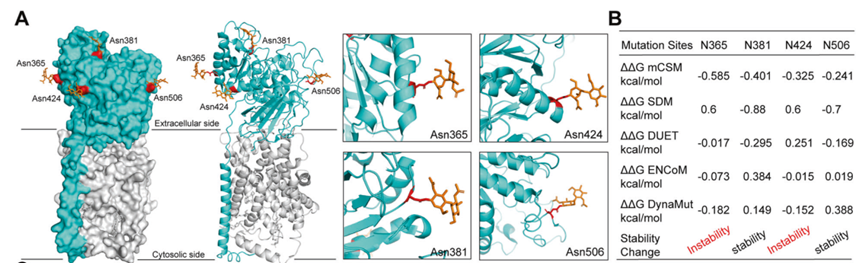
6. 4F2hc的N -糖基化是其膜定位和与xCT相互作用的必要条件
4F2hc与xCT分别是谷氨酸-胱氨酸逆向转运系统Xc-的重链与轻链。. 在野生型亲本PANC-1和MIA PaCa-2细胞中观察到4F2hc和xCT的共表达和膜共定位,但在衣霉素处理细胞中随着CHX(cycloheximide,一种蛋白合成抑制剂)处理时间的延长而显著降低。在RSL3处理的PANC-1细胞中,4F2hc的荧光强度增强;但在与RSL3共处理或不共处理的衣霉素处理PANC-1细胞中,4F2hc的表达和与xCT的膜共定位在很大程度上被抑制。研究人员随后证实,阻断4F2hc的N -糖基化可减弱其膜表达和与xCT的相互作用,从而赋予PDAC细胞对铁死亡的敏感性。
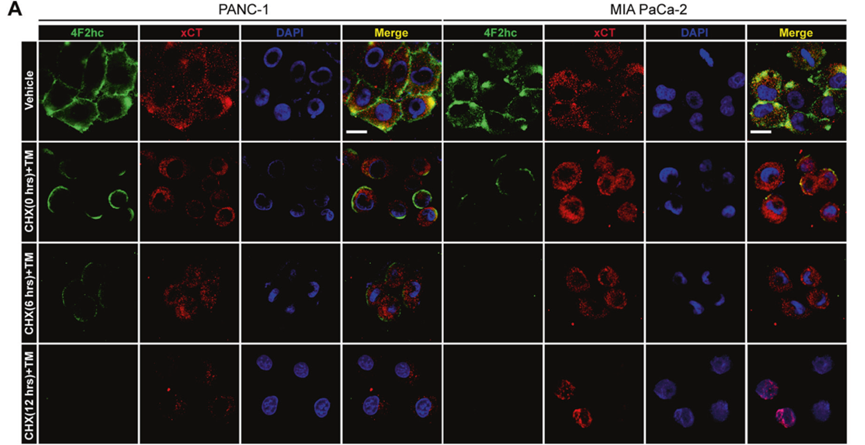
7. 衣霉素暴露通过部分抑制N -糖基化增加PDAC细胞对铁死亡的敏感性
衣霉素作为一种蛋白糖基化抑制剂,探讨衣霉素对PDAC细胞的潜在治疗价值,并评价衣霉素是否能显著增强PDAC细胞对铁死亡诱导剂的敏感性。咪唑酮铁死亡诱导剂 ( IKE)作为一种选择xc–系统抑制剂以及铁死亡诱导剂,4株经衣霉素处理的PDAC细胞株对RSL3或IKE诱导的铁死亡较未经衣霉素处理的PDAC细胞株更为敏感。此外的多项细胞研究结果都表明,靶向N-糖基化途径在PDAC的联合治疗中具有很大的潜力。
8. 体外和体内实验都表明B3GNT敲除限制了PDAC细胞的增殖能力
与野生型细胞相比,B3GNT3KO明显减弱了PANC-1和MIA PaCa-2细胞的自愈。Transwell实验显示B3GNT3KO PANC-1和MIA PaCa-2细胞的迁移和侵袭数量明显减少研究人员进行了体内和体外相关实验,结果显示,从肿瘤体积和肿瘤生长曲线来看,B3GNT3KO明显减缓了STTs和OTTs的生长。这些结果表明B3GNT3可能是一个主要参与PDAC进展的关键基因。
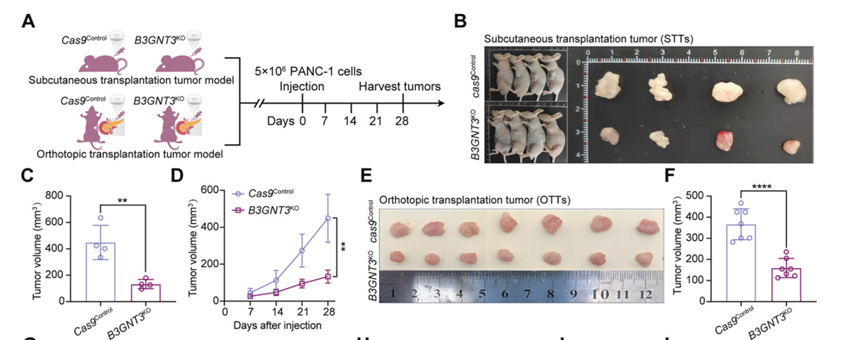
9. SLC3A2敲低可延缓PDAC细胞生长并增强IKE或衣霉素介导的PDAC抑制
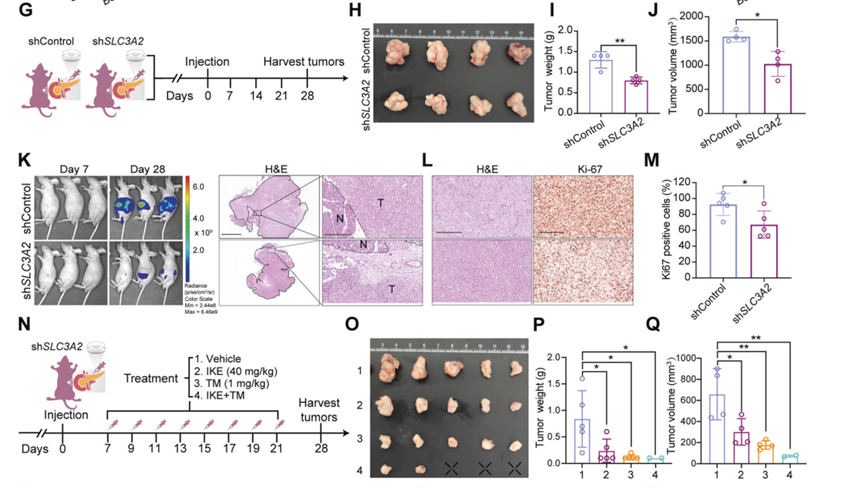
SLC3A2敲低可显著抑制PANC-1和MIA PaCa-2细胞的自愈,Transwell实验显示shSLC3A2 PANC-1和MIA PaCa-2细胞的迁移和侵袭受到显著抑制。OTTs模型和其他相关实验都证实,敲低SLC3A2可减缓肿瘤生长,降低肿瘤重量和体积,同时对小鼠体重无影响。这种抑瘤作用在用IKE或衣霉素治疗后可进一步显著增强。IKE和TM联合使用在很大程度上抑制了shSLC3A2 OTTs的肿瘤生长,但产生了不良的毒性,表现为小鼠体重明显减轻。这些结果表明,SLC3A2的敲低有助于PDAC的肿瘤抑制,并且与IKE或TM联合可大大增强这种抗肿瘤活性。
总结
在肿瘤药物开发的过程中,研究人员需要充分了解药物的作用机制和相关通路中关键蛋白,探索这些蛋白如何发挥作用。铁死亡是最近肿瘤治疗研究中的热点话题,通过对铁死亡关键通路,以及这些通路中蛋白在组织中的分布、共定位情况进行研究,可以帮助研究人员探索肿瘤中这些蛋白的作用情况,选择可能有效的潜在治疗方案。
Akoya Biosciences的多重免疫荧光技术可以帮助研究人员在一张切片上同时检测更多的蛋白标记物,了解这些标记物的相互作用情况,在组织中的分布位置,甚至可以帮助研究人员评估药物作用前后肿瘤微环境的变化。
参考文献
1.Ma, H., Chen, X., Mo, S. et al. Targeting N-glycosylation of 4F2hc mediated by glycosyltransferase B3GNT3 sensitizes ferroptosis of pancreatic ductal adenocarcinoma. Cell Death Differ 30, 1988–2004 (2023).

更多资讯请关注“云准科技”公众号
关于云准
云准医药科技(上海)有限公司(Accuramed Biotechnology Co., Limited)成立于2016年,是一家围绕疾病生物学研究、药物研发、新型诊断技术开发和公共卫生群体研究领域,专注于给科研机构和企业提供单细胞测序、空间多组学和蛋白质组学研究等科研服务,致力于用科技推动全民健康领域的发展。我们已经在疾病机理机制研究、药物新靶点发现、生物标记物开发、药物机理机制研究、临床前和临床研究以及临床检测等领域与众多客户产生合作,合作方向涉及肿瘤、免疫、慢病、罕见病等诸多方向以及公共卫生等人类健康领域。未来,云准将以创新为驱动力,继续对产品进行深度整合与开发,推动慢病诊疗、罕见病研究、肿瘤免疫治疗、病理诊断技术以及药物开发领域的突破性发展,必将为这些领域带来革命性变化。